Los peligros que presenta el uso y manipulación de estos productos para la salud, han motivado la adopción de una serie de normas de seguridad (por ejemplo, los límites permisibles de concentración de productos químicos en el trabajo) para evitar enfermedades e intoxicaciones a los operarios que los utilizan.
Origen
A los inhalantes de uso industrial se les llama solventes en virtud de su capacidad para disolver muchas otras sustancias . Con la introducción del uso del petróleo y sus derivados durante el siglo XX, cada vez son más los productos comerciales que contienen estos psicoactivos(sustancia química de origen natural o sintético que afectan específicamente las funciones del Sistema Nervioso Central (SNC), compuesto por el cerebro y la médula espinal): diluyentes, pegamentos, limpiadores, gasolinas, engrasantes, etc. Algunos investigadores aseguran que su inhalación con fines recreativos comenzó a partir de la década de los sesentas con la diseminación de los pegamentos para aereomodelismo.
Definición de solvente
Sustancia que es capaz de destruir la agregación de las moléculas de un cuerpo soluble. Un significado más amplio de la palabra es aquel componente que se halla en mayor proporción en una mezcla homogénea.
¿Qué son los solventes orgánicos?
Son compuestos orgánicos volátiles basados en el elemento químico Carbono. Se utilizan solos o en combinación con otros agentes para disolver materias primas, productos o materiales residuales, utilizándose para la limpieza, para modificar la viscosidad, como agente tensoactivo, como plastificante, como conservante o como portador de otras sustancias que una vez depositadas, quedan fijadas evaporándose el disolvente. En general, los disolventes orgánicos son de uso corriente en las industrias para pegar, desengrasar, limpiar, plastificar y flexibilizar, pintar y lubricar.
Entre la gran variedad de estas sustancias que se emplean en ámbitos industriales y domésticos, existe una amplia relación de disolventes orgánicos considerados tóxicos y muy tóxicos (ver Cuadro 2).
Características
Los disolventes industriales presentan las siguientes características principales:
-Son compuestos líquidos y de peso molecular ligero.
-Son sustancias poco polares, y por tanto escasamente miscibles en agua, que manifiestan una gran lipofilia.
-Poseen gran volatilidad, por lo que presentan una alta presión de vapor, pudiendo pasar fácilmente a la atmósfera en forma de vapor durante su manejo y por ello susceptibles de ser inhalados fácilmente.
-Tienen unos puntos de ebullición relativamente bajos.
-En general son mezclas de varios compuestos químicos mayoritarios acompañados de trazos de otros.
-Su composición puede variar con el tiempo, dada su volatilidad y elevada presión de vapor y por el hecho de que se contaminan con el uso.
-Uso muy amplio y diverso.
-En general, producen importantes efectos tóxicos.
Clasificación general
En los disolventes líquidos distinguimos:
Acuosos: usados para disolver sustancias polares. Sus propiedades físicas son las mismas del H2O y las químicas dependen de las sustancias que contengan.
Orgánicos: sustancias químicas o mezcla de las mismas, que son capaces de disolver sustancias no hidrosolubles y que por sus propiedades disolventes tienen múltiples aplicaciones en diversas tecnologías industriales-laborables. Los incluidos en este grupo son los considerados propiamente como disolventes.
Clasificación química
Hidrocarburos:
· Hidrocarburos simples.
-Cadena abierta saturados: alifáticos, alcanos, parafinas.
-Cíclicos saturados: cicloalcanos, cicloparafinas.
-Cíclicos no saturados: aromáticos.
-Derivados de los hidrocarburos: sustituyen algún hidrógeno.
-Halogenados.
-Funcionales: alcoholes, polialcoholes, éteres, ésteres, aldehídos, cetonas y epoxi.
-Nitroderivados: aminoderivados, amidoderivados.
-No hidrocarburos.
Disolventes hidrocarbonados o hidrocarburos: aquéllos cuyo núcleo básico elemental es el carbono y el hidrógeno (CH4), que pueden encadenarse entre sí de forma saturado o no, formando cadenas abiertas o cerradas con derivados, al sustituir algún hidrógeno por grupos funcionales o por átomos generalmente de halógenos (cloro, yodo, bromo o flúor).
Disolventes no hidrocarbonados: aquéllos cuyo elemento básico no es el hidruro de carbono (CH4). El único disolvente industrial que no es hidrocarbonado es el disulfuro de carbono (CS2).
También cabe diferenciar dentro de los disolventes:
-Disolventes puros: con un solo compuesto químico puro.
-Disolventes simples: con un solo compuesto generalmente no puro por contener impurezas de otros.
-Disolventes compuestos o mezclas: contienen mezclados varios disolventes de forma intencionada para las diferentes aplicaciones.
|
| |
| Grupo Químico | Nombre de los Solventes |
| Aromáticos | Benceno*, Tolueno, Xileno, Etilbenceno, Estireno |
| Hidrocarburos
| Tricloroetileno, Tetracloroetileno, Metilcloroformo
|
| Alcoholes | Alcohol Mitilico, Alcohol Isopropilico, Alcohol Butilico |
| Eteres | Dietil Eter, 1, 4-Dioxano |
| Esteres | Metil Acetato, Etil Acetato, Butil Acetato |
| Derivados del Glicol | Etilenglicol (Monoetil, Monometil, Monobutil Eter) |
| Clorofluorocarbonos | Fluorotriclometano (CFC-11), 1, 1, 2- Tr 1 Cloro 1,2,2- Trifluoroetano (CFC-113) |
| Misceláneas | n-Hexano, Disulfuro de Carbono, Dimetilfurmamida |
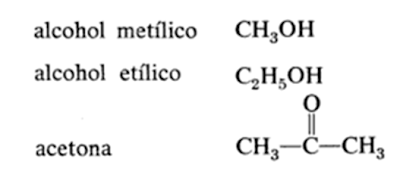
Química de identificación
 pegamentos (tolueno, acetato de etilo y varias acetonas), el thíner (destilados de petróleo, benceno, acetona, tricloroetileno, tetracloroetileno) y los removedores de barniz o pintura (acetona, tolueno, benceno, cloruro de metileno).
pegamentos (tolueno, acetato de etilo y varias acetonas), el thíner (destilados de petróleo, benceno, acetona, tricloroetileno, tetracloroetileno) y los removedores de barniz o pintura (acetona, tolueno, benceno, cloruro de metileno).
Los cosolventes y los solventes latentes sirven para realzar la capacidad de las resinas, aunque al combinarse con los solventes activos, actúan como catalizadores del secado (metanol, n-butanol, etc.)
Los diluyentes son elementos químicos que se utilizan únicamente porque bajan los costos del producto que se esté aplicando, ya que en la mayoría de los casos no desarrollan ningún efecto solvente por sí mismos (heptano, benceno, tolueno, xileno, etc.).
| | |
| Solventes de uso común | |
| PRODUCTOS | COMPOSICIÓN |
| Pegamentos y colas :
| Tolueno y acetona
|
| Insecticidas, odorizantes:
| Diversos fluorocarbonos |
| Carburantes :
| Hidrocarburos alifático
|
| Quitamanchas :
| 1,2 diclororopano
|
Formas de adulteración
Al ser productos de venta común sometidos a controles de calidad, no son susceptibles de adulteración.
Los usos más importantes de solventes orgánicos incluyen:
*Usos en limpieza y desengrasado de piezas de maquinaria, metales, plásticos y textiles.
*Usos en limpieza en seco.
*Constituyentes de pinturas, barnices, ceras, abrillantadores de zapatos y suelos, tintas, adhesivos.
*combustibles para motores, anticongelantes, productos farmacéuticos y conservantes de tejidos.
*Usos en el proceso de fabricación de gomas artificiales, cueros, plásticos, textiles y explosivos.
*Parte de fórmulas terapéuticas, desinfectantes.
*Parte de pesticidas, plaguicidas y herbicidas.
*Usos en procesos de extracción de grasas, aceites y sustancias
medicinales de semillas, frutos secos y huesos.
*Usos en diferentes reacciones químicas y procedimientos de
laboratorio.
�� diclorometano
�� tetracloroetileno
�� tricloroetileno
�� tolueno
�� xileno
�� 2-propanol
�� nafta
�� n-hexano
�� butiletilen glicol
�� CFC 113
�� white spirit (mezcla de hidrocarburos y parafinas)
Polaridad
Principales propiedades físicas de los solventes orgánicos

• Altamente inflamables: en 23ºC y menos.
• Inflamables: entre 23 y 61ºC
• De baja inflamabilidad: en más de 61ºC
Aunque hay que tener en cuenta el punto de inflamabilidad, la presión de vapor y otras propiedades, cuanto mayor sea la diferencia entre LEL y UEL, mayor será el riesgo de explosión o inflamabilidad, puesto que existirá un mayor rango de concentraciones a la cual el gas es peligroso. Así, únicamente según los datos expuestos en la Tabla 5, el Eter presenta mayor riesgo de fuego que el Tricloroetano.
Enlace: http://solvdb.ncms.org
En esta página web se encuentra una gran base de datos de solventes orgánicos y sus propiedades físicoquímicas así como mucha más información.
Pasos para acceder:
1. Dentro la página web hacer click en la opción "SOLV-DB".
2. Hacer click en la opción "SOLVENT NAME".
3. Para finalizar se busca el nombre del solvente del cual se desea conocer información.
Tipos de solventes y sus aplicaciones
Benceno:

Entre sus usos está el de disolvente, antiséptico y reactivo de síntesis química, se utiliza para degradar soluciones de alcohol etílico.
La forma más común de intoxicación es la inhalación de sus vapores.
Etilenglicol (1,2-etanediol):
Entre los usos se encuentran: Anticongelante de circuitos de refrigeración de motores combustión interna, difusor de calor, disolvente (pinturas, tintas, plásticos), síntesis de explosivos y de plásticos.
Formol (Formaldehído):
Dietil éter (éter sulfúrico):
Se absorbe rápidamente y eficazmente por vía respiratoria y digestiva. Se distribuye muy rápido en el tejido adiposo, S.N.C. Su proceso de biotransformación consiste en la hidrólisis de la unión éter, liberando dos moléculas de etanol.
Ampliamente utilizado en Química Industrial, ya sea como Solvente, o como materia prima para la síntesis. Como solvente su uso está relacionado con el tratamiento de Goma, Pintura, Lacas, y su principal uso como materia prima es para la síntesis de Fibra de Rayon.
| Solvente | Características | Usos y aplicaciones |
| Tolueno | Llamado también metilbenceno, líquido de olor parecido al del benceno, incoloro e inflamable; es un componente importante en el alquitrán de hulla, se obtiene en el fraccionamiento del petróleo. | Se usa para elevar el octanaje de gasolinas (gas avión); para la producción de beceno y fenol, como solvente para la elaboración de pinturas, resinas, recubrimientos, gomas, detergentes, químicos (ácido benzoico), perfumes, medicinas, sacarinas, etc. |
| Xileno | Dimetilbenzol, tiene tres isómeros (orto, meta y para); líquido inflamable, de olor semejante al del benceno, incoloro; se encuentra en el alquitrán de hulla. Se utiliza como disolvente u como diluyente. | Sus usos principales son: solventes para resinas, lacas, esmaltes, caucho, tintas, cuero, gasolina para aviación, agente desengrasante, producción de resinas epóxicas, elaboración de perfumes, producción de insecticidas y repelentes. |
| Acetato de Etilo | Líquido incoloro, fácilmente inflamable, hierve a 74- | Se recomienda su uso en laboratorios de fármacos. Se ocupa para la extracción líquida de antibióticos, en la industria de pinturas se ocupa como solvente activo para disolver las resinas sintéticas ocupadas en la formulación de estas. Otros usos son en la industria de fragancias, tintas, saborizantes, etc. |
| Acetato de Butilo | Líquido incoloro, fácilmente inflamable, hierve a 126.5ºC. | Se recomienda como disolvente y para aumentar el número de octanos. |
| Acetona | Líquido aromático, incoloro, inflamable, es la cetona más sencilla, importante como disolvente y medio de extracción. | Se emplea principalmente como disolvente en la fabricación de acetato de celulosa, pinturas, lacas y adhesivos, colorantes de la serie de la difenilamina, isopreno, piel artificial, mezclas adhesivas de nitrocelulosa, lubricantes, perfumes, productos farmacéuticos, plásticos, cementos ahulados, extracción de grasas y aceites, tónicos, purificación de parafina, etc. |
| Metil Isobutil Cetona | Líquido incoloro, inflamable y tóxico de olor parecido al de la acetona y el alcanfor. Es parcialmente soluble al agua, miscible en alcohol. | Se emplea en síntesis orgánicas, solventes de gomas, resinas, lacas de nitrocelulosa, producción de recubrimientos y adhesivos. |
| Metil Etil Cetona | Olor parecido a la menta (fragante y moderadamente penetrante), líquido incoloro, brillante, muy volátil y altamente inflamable, insoluble en agua. | Es utilizado en la producción de disolvente para revestimiento, adhesivo, cintas magnéticas, separación de la cera de los aceites lubricantes, tintas de imprenta, cuero sintético, papel transparente, papel aluminio, lacas, quitagrasas, extracción de grasas, aceites, ceras y resinas sintéticas y naturales. |
| Metanol | Líquido incoloro de olor característico, soluble en acetona, esteres. Arde con llama débilmente luminosa y es miscible con agua en todas las proporciones. | Se usa como solvente industrial, fabricación de formol, acetato de metilo y plastificantes. Como aditivos para gasolinas. Solvente en fabricación de colesterol, estreptomicina, vitaminas y hormonas, desnaturalizante para alcohol etílico. En la industria en general se usa como solvente en la fabricación de lacas, películas, plásticos, jabones, textiles, cuero artificial. En la preparación de removedores de pinturas, barniz, para soluciones anticongelantes. |
| Isopropanol | Líquido incoloro de olor característico al alcohol, parecido al alcohol etílico, pero más tóxico, sustituye al alcohol en preparados de cosmética y es importante como disolvente de lacas y como conservante. | Se emplea en linimentos, lociones para la piel, tónico para el pelo, preparación en ondulados permanentes, como solvente en procesos de extracción, anticongelantes, jabones líquidos, limpiadores y adelgazadores para pinturas, en la producción de glicerol, acetato de etilo, acetona, resinas, síntesis orgánicas, etc. |
| Gas nafta | Líquido incoloro, aromático, muy poco soluble en agua. | Como solvente para pinturas y diversos usos industriales, como desmanchador en tintorerías. |
| Nafta Deodorizada | Líquido incoloro, aromático, muy poco soluble en agua. | Como solvente para pinturas, ceras para calzado, diversos usos industriales y como principal uso, desmanchador en tintorerías de lavado en seco. |
| Gasolina Blanca | Líquido incoloro de olor a petróleo, insoluble en agua. | Se emplea principalmente como solvente para esmaltes alquidalicos, asfalto, barnices y para resinas naturales. Como agente limpiador y desengrasante, es solvente para grasas y aceites. Su función principal como combustible. |
| Heptano | Líquido incoloro con olor característico de las gasolinas, soluble en alcohol, éter y cloroformo. | Se emplea como sustituto del hexano en la extracción de aceites, en la elaboración de reactivos de laboratorio; como solvente para pinturas y en la industria papelera, como anestésico, para la preparación de adelgazadores y adhesivos como estándar para la determinación del octanaje en gasolinas, solvente para selladores y tintas. |
| Hexano | Líquido inflamable, volátil e incoloro, componente de la gasolina y del petróleo, olor ligeramente aromático, soluble en alcohol, acetona y éter. | Se usa especialmente como extractor de aceites vegetales, para efectuar reacciones de polimerización, como diluyente de pinturas, solventes en la preparación de adelgazadores, como alcohol desnaturalizado. Como materia prima para síntesis orgánicas, en la elaboración de thinners. |
| Percloroetileno | Líquido incoloro de olor característico | Se usa como solvente en desengrasado de metales, lavado de ropa en seco y en la fabricación de jabones. |
| Cloruro de Metileno | Líquido volátil, incoloro, de olor dulce agradable. Poco soluble en agua pero miscible en la mayoría de los disolventes orgánicos. Es prácticamente inflamable y no explosivo en condiciones normales de utilización. | Se emplea principalmente como disolvente, tanto en eliminación de pinturas y barnices como en su fabricación. Otras aplicaciones incluyen la fabricación de aerosoles para agroquímica y limpieza doméstica. |
| Butil Cellosolve | Líquido incoloro de suave olor característico, siendo dentro de los éteres de glicol de los de alto punto de ebullición, es ampliamente empleado como solvente retardador para lacas, nivelador de película en tintas, completamente soluble en agua. | Solvente para resinas de nitrocelulosa, lacas en spray, lacas de secado rápido, barnices, en textiles para prevenir las manchas de impresión o tejido, solvente para aceites minerales, para detener los jabones en solución ayudando a mejorar las propiedades emulsificantes, en general un solvente inerte, retardador en adelgazadores, agente acoplante. |
| Thinner Standard | Líquido incoloro de olor a petróleo, insoluble en agua. | Se emplea principalmente como adelgazador de pinturas automotrices, selladores, lacas para madera y primarios. Como limpieza y desengrasante de piezas mecánicas, limpieza de carburadores, etc. |
En el siguiente video se muestran algunos solventes y sus aplicaciones.
Prevención en su uso
*El trabajador y el supervisor del área deben conocer el tipo de solvente que están manipulando.
*En los centros de trabajo u otros locales en que se usen solventes se debe contar siempre con una ventilación adecuada.
*La concentración de los solventes en la atmósfera que se respira debe ser verificada periódicamente.
*Se puede instalar campanas extractoras que eviten el escape de los vapores de solventes hacia dirección del operador. Otra solución es trabajar con ductos extractores.
*Cuando sea inevitable la elevada concentración en el aire se debe usar mascarillas conectadas a un sistema de suministro de aire.
*Es indispensable una vía de escape segura hacia un lugar ventilado, para casos de emergencia.
*Se requiere tener contacto cutáneo con el solvente se puede usar guantes protectores de neopreno u otro que especifique el fabricante.
Los solventes orgánicos como material nocivo o potencialmente tóxico que con frecuencia se manipula en las labores industriales e inadvertidamente en el hogar pueden alcanzar el sistema nervioso central o periférico después de haber sido inhalados y absorbidos por la sangre. Según sea la sustancia, el tiempo y el grado de exposición pueden reducir, o incluso destruir las funciones de las células nerviosas, alterar la función renal, hepática, de la médula ósea, etc. Al margen de la vía de ingreso a nuestro organismo que puede ser también a través de la piel.
En las mucosas, principalmente las oculares y respiratorias, por contacto con los vapores, produce una acción irritante, aunque las conjuntivas oculares pueden verse afectadas por salpicaduras accidentales. Producen en los centros nerviosos un efecto bipolar de excitación-depresión muy similar a los agentes anestésicos. Sus efectos se exteriorizan con signos y síntomas de somnolencia y ebriedad.
Reciclaje
En la actualidad existen métodos de reciclado de disolventes que son capaces de recuperar aproximadamente el 90% del volumen original de los líquidos. De esta forma se reutilizan los disolventes y se produce una menor contaminación.
El funcionamiento de la máquina de reciclado es relativamente sencillo: se coloca el disolvente sucio en un tanque de teflón cubierto con tapa de acero inoxidable. Mediante un termostato se hace subir la temperatura del disolvente por encima del punto de ebullición. El líquido se volatiliza y pasa a un condensador, que se enfría con aire, donde se concentra el disolvente y se vuelve a reutilizar.
Enlaces:
http://www.chemtools.com.pe/productos.php?option=5
www.higieneocupacional.com.br/download/solventes-organicos.ppt
http://solvdb.ncms.org












Hola. Me parece que si organizaran este blog por entradas, les saldría mucho mejor, también si pudieran arreglar lo de las imágenes y ese código rarazo. Atte. PERCY LEITH - LOS ANFÓTEROS.
ResponderEliminarTambién podrían explicar las propiedades fisicoquímicas de los solventes (Viscocidad, fuerzas intermoleculares, poder disolvente, etc...) y de paso explican cómo estas actúan al momento de disolver.
ResponderEliminarBARRIENTOS:lo mas resaltante que encontre fue la metodo tan sencillo de reciclaje de los solventes y con un buen redimiento
ResponderEliminarel blog nos brinda una buena informacion la clasificacion de solventes con respecto a su grupo funcional y sus aplicaciones en la industria y tener un video sobre reciclado de estos para obtener una menor contaminacion
ResponderEliminarel blog nos brinda una buena informacion la clasificacion de solventes con respecto a su grupo funcional y sus aplicaciones en la industria y tener un video sobre reciclado de estos para obtener una menor contaminacion
ResponderEliminarHola su blog esta interesante pero creo que seria mas adecuado poder separar su informacion mediante entradas disponibles, y creo que la prevencion y reciclaje es lo que mas resalta ya que nos da a conocer como poder volver a utilizar el mismo solvente y tambien para no contaminar mas el medio ambiente ya que algunos solventes son toxicos.
ResponderEliminarhola,interezante aporte sobre el reciclado de solventes en el blog,por que así ayuadamos a la menor contaminación ambiental y se haría mas conveniente el uso de solventes en la industria,por su mayor rendimiento.
ResponderEliminarYessica Antaurco.R
Video interesante,pero algo reducida la informacion, no es bueno que solo se vea un posteo en un blog,las entradas son precisamente para eso, de forma que lo puedan hacer como libro.
ResponderEliminarCon resepecto a la informacion, rescatable lo de reciclaje y los links(ojo,paginas ajenas no deben quitarle protagonismo a su blog)
Puede quedar mejor
JESSE ZORRILLA, al parecer no encontramos reacciones escensiales de los solventes , de como, con cuales compuestos podemos encontrar una interaccion, nos muestran nombres de compuestos mas no sus formulas, pero se observa buenos videos de reciclaje muy importante ahora en el calentamiento global. Gracias
ResponderEliminarPamela.
ResponderEliminarMe parece de gran importancia eso de las propiedades explosivas de los solventes, LEL,UEL, para evitar accidentes de ese tipo.
Sobre el reciclaje de solventes industriales, el video es interesante, gracias a ese tipo de procesos al menos se esta haciendo aunque poquito q el avance de la destruccion del planeta sea mas lento.
ah¡¡ .. saben hay muchos links.. eso hace q su blog pierdaa en algo su escencia, bueno en particular no me gusta mucho ..
ResponderEliminarEste comentario ha sido eliminado por el autor.
ResponderEliminarEn primer lugar, me parece que su blog es muy extenso, se hace aburrido de leer, tal vez deberian pensar en hacer varias entradas en vez de una sola muy larga. Me parece interesante la información sobre los límites de explosividad, así como lo del reciclaje, que es una alternativa para disminuir la contaminación ambiental. Falto informacion de mezclas de solventes.
ResponderEliminarA los que no tienen nuestro blog,
ResponderEliminarwww.grupopetroquimica.blogspot.com
Muchos temas son interesantes,en especial el de reciclaje,aunque falta un poco mas de informacion; y ordenarlos por entradas seria mucho mejor.
ResponderEliminarMe parece que su informacion es buena; sin embargo, debieron clasificarla en entradas o categorias especificas. Resalto lo interesante del video y el reciclado de solventes.
ResponderEliminarVELA:Muy buena la informacion pero hubiese sido mejor mostrar esa informacion por entradas,usen todas las herramientos que le permite el blog.
ResponderEliminarQuizas hubiesen tratado de mostrar las formulas y estructuras moleculares de los compuestos.Lo que me parecio muy bueno tambien fue de los links, si bien es cierto no todo puedes explicar aca los links nos ayudan bastante para profundizar.
Si pz ver lo que los solventes logran contra el medio ambiente es bastante ... mucha responsabilidad acerca de los malos maejos de ellos
ResponderEliminarEl etielnglicol como usteden lo dicen Anticongelante de circuitos de refrigeración de motores combustión interna... en lo q respecta a desengrasantes tb es muy utilizado... algo mas acerca de los solventes biodegradables hubiera sido un buen aporte ... es un blog que busca el cuidado del medio ambiente MUY BIEN!!!
ResponderEliminarLa variedad de solventes que han sido descritos y caracterizados dan un panorama más claro sobre solventes en general. Estoy de acuerdo con el buen aporte dado sobre la información de reciclaje. A medida de crítica constructiva, el blog podría organizarse mejor anexando entradas y etiquetas.
ResponderEliminarJesse Zorrilla, apreciamos como se usa el metodo de destilacion para reciclar solventes industriales, este metodo ya ha sido usado en laboratorios anteriores, esta claro que la destilacion es muy importante en la industria quimica, gracias
ResponderEliminarInteresante el trabajo, en la parte "origen de solventes" mencionaste algo que casi ningún grupo mencionó: "el uso de los disolventes en la drogadiccion". En estos casos, el disolvente es inhalado por el ser humano para provocar una modificación en la conciencia. Pero, lamentablemente no se puede hacer nada para frenar esta degradación, ya que los hidrocarbonos volátiles no están sujetos a ningún tipo de control internacional (son productos de venta legal). En algunos países hay restricciones sobre su venta a menores de edad y en otros se ha prohibido su inhalación aunque no su venta. En general, los productos que los contienen son muy fáciles de conseguir. Resalto lo dicho anteriormente, ya que los solventes industriales son utilidades de mala manera.
ResponderEliminarLa utilización de un video para tocar el tema de reciclado para disolventes de manera ilustrativa buena; pero el desarrollo del tema de solventes de manera general desordenada .
ResponderEliminarLa utilización de un video para tocar el tema de reciclado para disolventes de manera ilustrativa buena; pero el desarrollo del tema de solventes de manera general desordenada .
ResponderEliminar´TORRES´::La evaluación de riesgos también se usa para diseñar estrategias de prevención de riesgos para la salud humana,ya que el mal uso de estos solventes nos puede costar nustra propia vida(recuerdenlo).
ResponderEliminarel butilcellosolve lo puedo usar para realizar un aantiespumante
ResponderEliminarel butilcellosolve lo puedo usar para realizar un aantiespumante
ResponderEliminarel butilcellosolve lo puedo usar para realizar un aantiespumante
ResponderEliminarCreo que la lógica es parecida a los líquidos potenciadores de motor o para hace la combustión menos nociva para el medio ambiente. Al menos en el rubro de alquiler grupo electrogeno trabajamos también con algunos de estos principios activos, aunque hay que tener cuidado con las combustiones.
ResponderEliminarExcelente ayuda
ResponderEliminarlo que faltaba que enfermedades causaraian los votalis
ResponderEliminarmuy bueno
ResponderEliminarSÚPER. ME AYUDO EN EL TEMA DE LA DESNATURALIZACIÓN DE LAS PROTEÍNAS POR SOLVENTES ORGÁNICOS.
ResponderEliminarmr pedro email de contacto / whatsapp +18632310632 detalles, pedroloanss@gmail.com. eso me ayudó con un préstamo de 200.000,00 euros para poner en marcha mi negocio y estoy muy agradecido, fue muy duro para mí intentar abrirme camino como madre soltera las cosas no han sido fáciles para mí pero con la ayuda del sr. pedro Pon una sonrisa en mi cara mientras veo que mi negocio se fortalece y se expande también. Sé que puede que se sorprenda de por qué puse cosas como esta aquí, pero realmente tengo que expresar mi gratitud para que cualquier persona que busque ayuda financiera o que esté pasando por dificultades con su negocio o quiera comenzar un proyecto comercial pueda ver esto y tener la esperanza de salir de las dificultades .. gracias.
ResponderEliminar